Ung thư biểu mô đường mật, còn gọi là ung thư ống mật, là loại ung thư gan ít gặp hơn, xuất phát từ các ống dẫn mật từ gan đến ruột và túi mật.
Một loại ung thư gan rất hiếm gặp bắt nguồn từ các mạch máu ở gan là sarcoma mạch. U nguyên bào gan cũng là một loại ung thư gan hiếm gặp, đa số chỉ xuất hiện ở trẻ nhỏ.
Dịch tễ của ung thư gan
Theo Globocan 2020, tại Việt Nam có hơn 26.000 người được chẩn đoán ung thư gan, trong đó tỷ lệ nam giới mắc bệnh gấp hơn 3 lần so với nữ giới.
HCC thường xuất hiện ở những người bị tổn thương gan do béo phì, uống quá nhiều rượu, bị viêm gan B hoặc viêm gan C. Ung thư gan phổ biến ở các nước châu Á – Thái Bình Dương và châu Phi do tỷ lệ nhiễm viêm gan B cao.
Các triệu chứng của ung thư gan
 Người bị ung thư gan giai đoạn tiến triển có thể bị vàng da và vàng mắt. Nguồn ảnh: Healthcentral.com
Người bị ung thư gan giai đoạn tiến triển có thể bị vàng da và vàng mắt. Nguồn ảnh: Healthcentral.comUng thư gan thường không gây ra bất kỳ triệu chứng nào trong giai đoạn đầu. Tuy nhiên, các triệu chứng thường xuất hiện khi ung thư tiến triển hoặc lan rộng. Các triệu chứng phổ biến của ung thư gan là:
- Suy nhược và mệt mỏi
- Đau bụng, có thể lan lên vai phải
- Chán ăn và buồn nôn
- Sụt cân không rõ nguyên nhân
- Vàng da và vàng mắt (hội chứng hoàng đản)
- Nước tiểu sẫm màu và phân nhạt màu
- Ngứa da
- Dịch cổ trướng
- Sốt
Những triệu chứng này cũng có thể do các bệnh lý khác gây ra. Vì vậy, người bệnh nên đi khám khi xuất hiện một trong các triệu chứng này để loại trừ ung thư gan.
Yếu tố nguy cơ của ung thư gan
HCC, loại ung thư gan nguyên phát phổ biến nhất, thường liên quan đến bệnh viêm gan B và viêm gan C mạn tính.
Xơ gan cũng có thể làm tăng nguy cơ phát triển HCC. Các mô gan bị xơ làm giảm lượng máu đến gan và làm chậm quá trình chuyển hóa các chất dinh dưỡng, hormone, thuốc và các chất độc. Nó cũng làm chậm quá trình sản xuất protein và các chất khác ở gan.
Xơ gan có thể hình thành trong nhiều tháng hoặc nhiều năm và gây ra bởi một số yếu tố như:
- Viêm gan B hoặc viêm gan C
- Bệnh gan nhiễm mỡ, thường liên quan đến chế độ ăn nhiều carbohydrate, thừa cân hoặc béo phì, uống quá nhiều rượu hoặc mắc bệnh đái tháo đường típ 2
- Uống rượu (có hoặc không đi kèm bệnh gan nhiễm mỡ)
- Bệnh đái tháo đường típ 2 (có hoặc không đi kèm bệnh gan nhiễm mỡ)
- Một số rối loạn di truyền như bệnh rối loạn sắc tố di truyền (haemochromatosis) hoặc tình trạng thiếu hụt protein đặc biệt khiến mô phổi và mô gan bị phá vỡ (thiếu alpha-1 antitrypsin).
Hút thuốc lá cũng làm tăng nguy cơ phát triển HCC. Khả năng mắc ung thư gan càng cao nếu có nhiều hơn một yếu tố nguy cơ nêu trên.
Mối liên quan giữa viêm gan và ung thư gan
Trên thế giới, khoảng 80% trường hợp HCC có thể liên quan đến bệnh viêm gan B hoặc viêm gan C.
Viêm gan B và viêm gan C có thể lây lan khi tiếp xúc với máu, tinh dịch hoặc các loại dịch cơ thể khác của người bị nhiễm bệnh. Sự lây lan có thể xảy ra khi quan hệ tình dục với bạn tình bị nhiễm bệnh hoặc do dùng chung vật dụng cá nhân với người bị nhiễm bệnh như dao cạo râu, bàn chải đánh răng hoặc kim tiêm. Con đường lây lan phổ biến nhất của bệnh viêm gan B là lây từ mẹ sang con trong quá trình sinh đẻ.
Khi bị viêm gan, virus sẽ xâm nhập vào các tế bào gan và bắt đầu nhân lên. Khi đó, hệ thống miễn dịch của cơ thể sẽ tấn công virus và gây ra tình trạng viêm gan. Nếu viêm gan kéo dài hơn 6 tháng (viêm gan mạn tính), nó có thể dẫn đến xơ gan và làm tăng nguy cơ tiến triển thành ung thư gan.
Để hạn chế sự lây lan của viêm gan B và giảm tỷ lệ ung thư gan nguyên phát, những người có yếu tố nguy cơ cần được tiêm vắc-xin phòng viêm gan B, bao gồm:
- Bạn tình của những người mắc bệnh viêm gan B
- Trong gia đình có người bị viêm gan B
- Người thường xuyên phải truyền máu và các chế phẩm máu
- Trẻ sơ sinh và trẻ nhỏ
Nếu đã bị nhiễm viêm gan B, việc tiêm phòng sẽ không còn tác dụng nữa. Tuy nhiên, người bệnh cần phải đi khám định kỳ để đề phòng các bệnh lý ở gan. Nếu có dấu hiệu tổn thương gan do virus viêm gan B, người bệnh sẽ được chỉ định các loại thuốc kháng virus để kiểm soát hoạt động của chúng và ngăn tổn thương gan tiến triển.
Các loại thuốc kháng virus mới có thể chữa khỏi bệnh viêm gan C trong đa số trường hợp. Điều này làm giảm nguy cơ phát triển ung thư gan nhưng không thể ngăn chặn bệnh tuyệt đối. Sau khi đã điều trị viêm gan thành công, những người bị xơ gan vẫn cần được theo dõi lâu dài.
Chẩn đoán ung thư gan
Ung thư gan được chẩn đoán dựa vào một số xét nghiệm, bao gồm xét nghiệm máu và các xét nghiệm chẩn đoán hình ảnh như siêu âm, chụp cắt lớp vi tính (CT) và cộng hưởng từ (MRI). Trong một số trường hợp, bác sĩ có thể chỉ định sinh thiết gan để chẩn đoán ung thư.
Xét nghiệm máu
Xét nghiệm máu không phải là xét nghiệm để chẩn đoán xác định ung thư gan, nhưng chúng có thể là công cụ để hỗ trợ chẩn đoán. Một số xét nghiệm máu cần thiết là:
- Xét nghiệm chức năng gan
Xét nghiệm này đánh giá tình trạng hoạt động của gan. Nó có thể được thực hiện trước, trong và sau khi điều trị.
- Xét nghiệm đông máu
Đây là xét nghiệm giúp đánh giá khả năng sản xuất các protein đông máu của gan. Khả năng đông máu giảm có thể làm tăng nguy cơ chảy máu.
- Xét nghiệm virus viêm gan
Xét nghiệm này có thể phát hiện virus viêm gan B và virus viêm gan C. Đây là các loại virus có thể dẫn đến ung thư gan nguyên phát.
- Chất chỉ điểm ung thư
Chất chỉ điểm ung thư (Tumor marker) có thể được tạo ra bởi các tế bào ung thư. Chúng có thể hỗ trợ chẩn đoán một số loại ung thư. Chất chỉ điểm ung thư phổ biến nhất của HCC là alpha-fetoprotein (AFP). Đôi khi, nồng độ AFP vẫn có thể ở mức bình thường trong ung thư gan. Mặt khác, nồng độ AFP tăng không đồng nghĩa với việc bị ung thư gan. Một số trường hợp như mang thai, viêm gan và hội chứng vàng da cũng có thể tăng nồng độ AFP.
Xét nghiệm chẩn đoán hình ảnh
Xét nghiệm chẩn đoán hình ảnh phổ biến nhất được sử dụng để phát hiện ung thư gan là siêu âm ổ bụng. Siêu âm cũng được sử dụng để theo dõi tiến triển của xơ gan. Tuy nhiên, siêu âm không thể chẩn đoán xác định ung thư gan nên vẫn cần thực hiện các xét nghiệm khác.
- Siêu âm ổ bụng
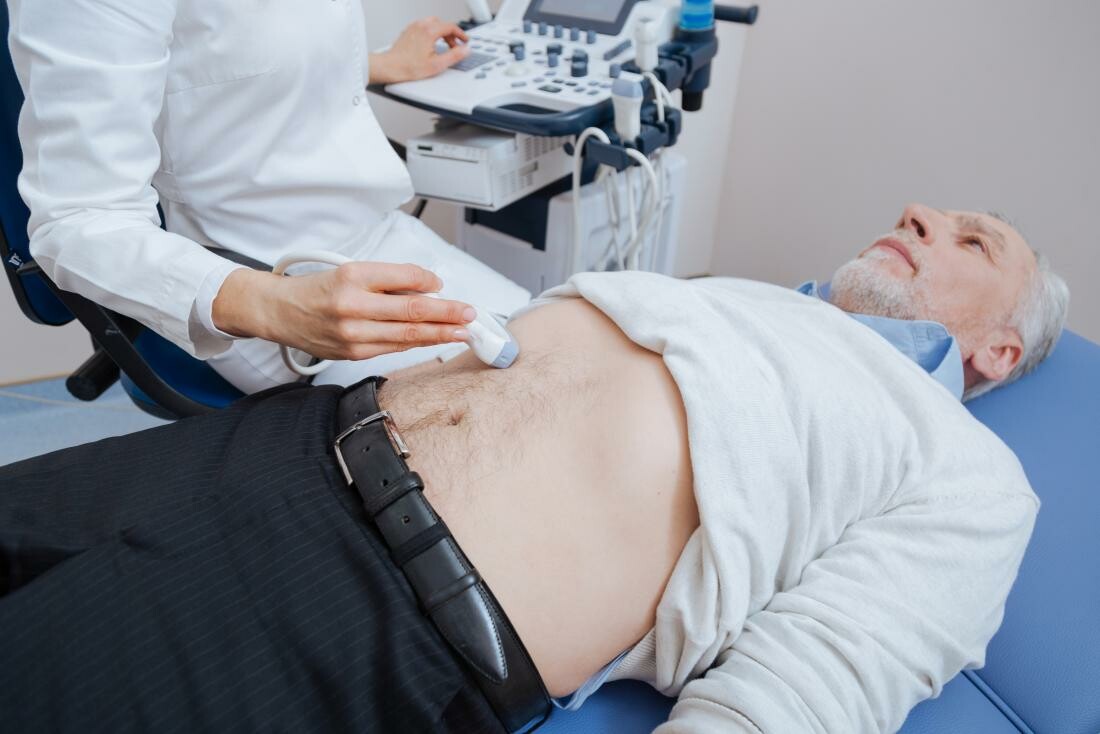 Siêu âm ổ bụng là một trong những xét nghiệm chẩn đoán hình ảnh hữu ích để phát hiện ung thư gan. Nguồn ảnh: Medicalnewstoday.com
Siêu âm ổ bụng là một trong những xét nghiệm chẩn đoán hình ảnh hữu ích để phát hiện ung thư gan. Nguồn ảnh: Medicalnewstoday.comSiêu âm ổ bụng là xét nghiệm chẩn đoán hình ảnh được sử dụng để phát hiện ung thư và đánh giá kích thước khối u.
Người bệnh sẽ được yêu cầu nhịn ăn (kể cả uống nước) trong khoảng 4 giờ trước khi siêu âm. Trong quá trình siêu âm, người bệnh sẽ nằm trên giường và kéo áo cao ngang ngực. Bác sĩ sẽ bôi một lớp gel lên da và di chuyển đầu dò khắp bụng. Sóng âm đi tới các cơ quan hoặc khối u sẽ dội ngược trở lại đầu dò. Bộ chuyển đổi xử lý các sóng phản xạ và mã hóa thành hình ảnh của các cơ quan hoặc khối u đó.
Siêu âm không gây đau và chỉ kéo dài trong khoảng 15 – 20 phút.
Nếu phát hiện khối u, bác sĩ sẽ chỉ định thêm các xét nghiệm chẩn đoán hình ảnh khác để xác định xem đó có phải là ung thư hay không. Các khối u gan lành tính thường được phát hiện nhờ siêu âm.
- Chụp cắt lớp vi tính
Chụp cắt lớp vi tính (CT scan) sử dụng tia X quét lên cơ thể theo các lát cắt ngang.
Khi chụp CT, thuốc cản quang sẽ được tiêm vào tĩnh mạch, đi vào máu và tập trung ở các vị trí bất thường. Tác dụng phụ của thuốc cản quang là gây đỏ bừng mặt và gây khó chịu ở bụng. Dù các triệu chứng sẽ nhanh chóng thuyên giảm nhưng người bệnh nên nói với bác sĩ nếu cảm thấy không khỏe sau khi tiêm thuốc cản quang.
Người bệnh sẽ nằm trên giường và được di chuyển qua máy chụp CT. Quy trình chụp CT thường kéo dài trong 15 – 20 phút.
- Chụp cộng hưởng từ
Chụp cộng hưởng từ (MRI) sử dụng sóng từ để tạo ra hình ảnh của các mặt cắt ngang qua cơ thể. MRI có thể đánh giá mức độ lan rộng và tình trạng xâm nhập mạch của khối u. Quá trình chụp MRI có thể mất từ 30 – 90 phút.
Thuốc cản quang cũng có thể được sử dụng trong quá trình chụp MRI. Nó có thể gây dị ứng. Nếu đã có phản ứng dị ứng với iốt hoặc thuốc cản quang trong lần chụp trước, hãy báo lại với bác sĩ. Ngoài ra, bạn cũng nên cho bác sĩ biết nếu bản thân mắc bệnh đái tháo đường, bệnh thận hoặc đang mang thai.
Sinh thiết gan
Sinh thiết gan là thủ thuật lấy một vài mảnh mô nhỏ ở gan để quan sát dưới kính hiển vi. Đây không phải là xét nghiệm bắt buộc để chẩn đoán ung thư gan nguyên phát vì chụp CT thường đã đủ để chẩn đoán, đặc biệt là ở những người bị xơ gan. Tuy nhiên, sinh thiết gan có thể được chỉ định nếu bác sĩ vẫn chưa chắc chắn về chẩn đoán sau khi chụp CT.
Trước khi sinh thiết gan, người bệnh sẽ được làm xét nghiệm đông máu vì gan có nhiều mạch máu, nguy cơ chảy máu cao khi làm thủ thuật. Có 2 phương pháp sinh thiết gan, bao gồm:
- Sinh thiết gan qua da
Bác sĩ sẽ gây tê vị trí chọc kim, sau đó đưa kim qua da bụng để lấy mảnh mô nhỏ từ khối u. Thủ thuật này thường kết hợp với siêu âm hoặc CT để xác định đúng vị trí khối u gan. Nếu có nguy cơ chảy máu cao, người bệnh có thể phải nằm viện trong vài giờ hoặc qua đêm để theo dõi tình trạng chảy máu.
- Sinh thiết nội soi
Trong thủ thuật này, người bệnh sẽ được gây mê toàn thân. Bác sĩ sẽ rạch một vài đường nhỏ ở bụng và đưa ống nội soi có gắn camera vào để quan sát gan và lấy mẫu mô. Thủ thuật này được thực hiện nếu bác sĩ nghi ngờ ung thư đã di căn đến các vị trí khác của cơ thể.
Các giai đoạn của ung thư gan
Thông qua các xét nghiệm nêu trên, bác sĩ sẽ xác định mức độ xâm lấn của ung thư gan. Ngoài ra, chức năng gan cũng sẽ được đánh giá dựa trên thang điểm Child-Pugh.
Thang điểm Child-Pugh
Thang điểm này đánh giá và phân loại mức độ tổn thương gan do xơ gan gây ra.
- Child-Pugh A: Gan hoạt động tốt và bệnh xơ gan ít tiến triển.
- Child-Pugh B: Gan hoạt động vừa phải.
- Child-Pugh C: Gan hoạt động kém và bệnh xơ gan đang tiến triển.
Hệ thống phân loại bệnh ung thư gan Barcelona (Barcelona Clinic Liver Cancer – BCLC) thường được sử dụng để phân chia giai đoạn HCC. Các tiêu chí dựa trên khả năng sinh hoạt hàng ngày, giai đoạn của khối u và chức năng gan. Xác định giai đoạn theo BCLC sẽ giúp bác sĩ đưa ra kế hoạch điều trị tốt nhất.
Hệ thống phân loại ung thư gan nguyên phát theo BCLC
- Giai đoạn 0 (giai đoạn rất sớm): 1 khối u đơn lẻ, kích thước dưới 2 cm; Child-Pugh A
- Giai đoạn A (giai đoạn sớm): 1 khối u hoặc tối đa 3 khối u, tổng kích thước dưới 3 cm; Child-Pugh A – B
- Giai đoạn B (giai đoạn trung bình): Nhiều khối u ở gan; Child-Pugh A – B
- Giai đoạn C (giai đoạn tiến triển): Ung thư đã xâm lấn mạch máu, di căn đến các hạch bạch huyết hoặc các cơ quan khác của cơ thể; Child-Pugh A – B
- Giai đoạn D (giai đoạn cuối): Child-Pugh C, khối u với mọi kích thước
Tiên lượng của ung thư gan
Không thể xác định chính xác bệnh ung thư gan sẽ diễn biến ra sao. Tuy nhiên, bác sĩ có thể đưa ra tiên lượng bệnh để dự đoán khả năng tiến triển của ung thư.
Để đưa ra tiên lượng bệnh, bác sĩ sẽ cân nhắc:
- Kết quả của các xét nghiệm
- Loại ung thư gan mà người bệnh mắc
- Giai đoạn của ung thư và tốc độ tiến triển bệnh
- Tình trạng xơ gan và chức năng gan
- Khả năng đáp ứng điều trị
- Các yếu tố khác như tuổi tác, thể lực và sức khỏe tổng thể của người bệnh
Tiên lượng bệnh có thể tốt nếu ung thư gan vẫn còn ở giai đoạn đầu. Tuy nhiên, ung thư gan thường được phát hiện muộn nên tiên lượng bệnh khá dè dặt. Bác sĩ thường sử dụng số liệu được thống kê qua các nghiên cứu để đánh giá tiên lượng của người bệnh. Số liệu này phản ánh kết quả điều trị xảy ra phổ biến nhất với đa số người bệnh. Mặc dù số liệu thống kê cung cấp cho bác sĩ cái nhìn tổng quát về tiến triển bệnh nhưng nó không phản ánh chính xác về tình trạng của từng người bệnh.
Ghép gan hoặc phẫu thuật cắt gan là phương pháp điều trị phù hợp với một số trường hợp ung thư gan nguyên phát. Các phương pháp điều trị khác có thể làm tăng đáng kể tỷ lệ sống và làm giảm các triệu chứng của ung thư, giúp cải thiện chất lượng cuộc sống của người bệnh.
Điều trị ung thư gan
Điều trị ung thư gan phụ thuộc vào kích thước, vị trí, tình trạng xâm lấn mạch máu của khối u và chức năng gan của người bệnh. Bác sĩ cũng sẽ cân nhắc đến tuổi tác, sức khỏe tổng thể của người bệnh và các phương pháp điều trị phù hợp.
Các phương pháp điều trị HCC theo giai đoạn
Đa số các trường hợp HCC sẽ được chỉ định phương pháp đốt nhiệt bằng sóng cao tần hoặc nút mạch hóa chất. Phẫu thuật được chỉ định với khoảng 5% người bệnh.
- Giai đoạn 0 (giai đoạn rất sớm): thường điều trị bằng phương pháp phẫu thuật cắt gan
- Giai đoạn A (giai đoạn sớm): thường là đốt nhiệt bằng sóng cao tần, nút mạch hóa chất, phẫu thuật cắt gan hoặc ghép gan
- Giai đoạn B (giai đoạn trung bình): sử dụng nút mạch hóa chất
- Giai đoạn C (giai đoạn tiến triển): sử dụng liệu pháp nhắm trúng đích hoặc điều trị chăm sóc giảm nhẹ
- Giai đoạn D (giai đoạn cuối): điều trị chăm sóc giảm nhẹ hoặc tham gia các thử nghiệm lâm sàng; một số người bị suy gan và có khối u nhỏ có thể được chỉ định ghép gan.
Phẫu thuật cắt gan
Mục đích của phẫu thuật cắt gan là loại bỏ phần gan có ung thư. Chỉ một số ít người bị ung thư gan được chỉ định phẫu thuật vì nó không áp dụng cho những trường hợp ung thư gan đã xâm lấn mạch máu. Chức năng gan cũng cần đảm bảo để gan có thể tự phục hồi sau phẫu thuật. Những người không bị xơ gan hoặc bị xơ gan ở giai đoạn sớm có thể được cân nhắc phẫu thuật cắt gan. Xơ gan giai đoạn nặng không có chỉ định phẫu thuật cắt gan.
Các phương pháp phẫu thuật cắt gan
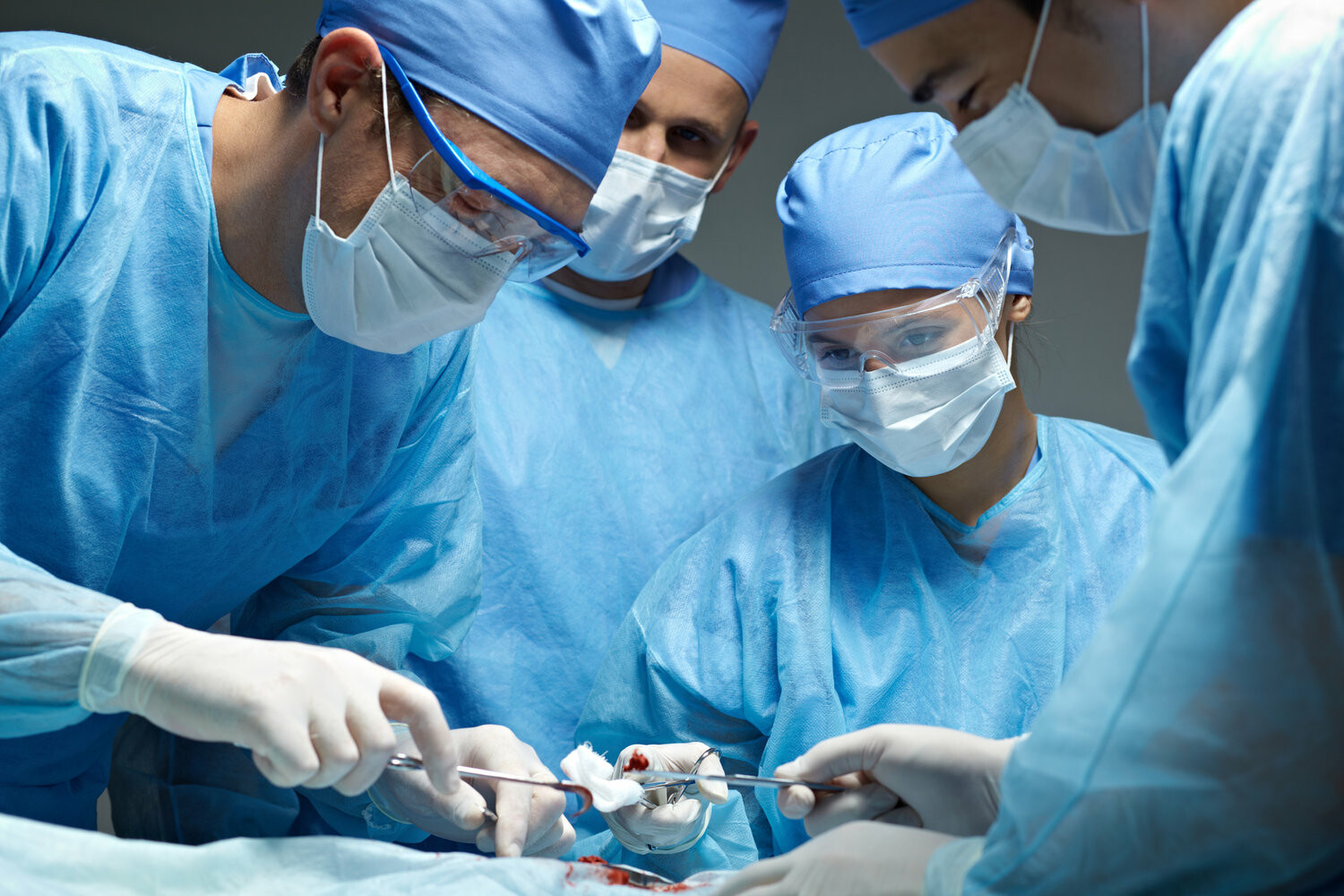 Phẫu thuật cắt gan có thể được chỉ định trong một số trường hợp ung thư gan. Nguồn ảnh: Drdavidjoseph.com.au
Phẫu thuật cắt gan có thể được chỉ định trong một số trường hợp ung thư gan. Nguồn ảnh: Drdavidjoseph.com.auCó nhiều phương pháp phẫu thuật cắt gan khác nhau, tùy thuộc vào kích thước và vị trí của khối u. Đôi khi, túi mật cũng có thể bị cắt bỏ cùng với một phần của cơ hoành (cơ ngăn cách lồng ngực với ổ bụng).
- Phương pháp phẫu thuật
Đa số phẫu thuật cắt gan là phẫu thuật mở với đường mổ lớn ở bụng. Bên cạnh đó, phẫu thuật cắt gan nội soi qua các đường rạch nhỏ hiện nay cũng ngày càng phổ biến hơn. Bác sĩ sẽ đưa ống nội soi có gắn camera qua đường rạch nhỏ. Ống nội soi có gắn thêm dụng cụ phẫu thuật để bác sĩ cắt bỏ gan.
Phẫu thuật nội soi ít gây đau hơn, thời gian nằm viện ngắn hơn và khả năng hồi phục nhanh hơn so với phẫu thuật mở. Tuy nhiên, phẫu thuật nội soi không phù hợp với tất cả các trường hợp và không phải bệnh viện nào cũng thực hiện được. Cho dù phẫu thuật mở hay phẫu thuật nội soi thì cắt gan vẫn là một phẫu thuật lớn. Người bệnh sẽ được gây mê toàn thân, sau đó bác sĩ sẽ cắt bỏ khối u và một phần mô gan khỏe mạnh xung quanh.
- Sau khi phẫu thuật
Phần gan còn lại sẽ bắt đầu phát triển, kể cả khi đã cắt bỏ ¾ gan. Gan thường phát triển trở lại kích thước bình thường trong vòng vài tháng, mặc dù hình dạng của gan có thể thay đổi một chút.
Biến chứng thường gặp nhất sau khi phẫu thuật là chảy máu vì có rất nhiều mạch máu ở gan. Bác sĩ sẽ theo dõi các dấu hiệu chảy máu và nhiễm trùng. Ngoài ra, một số người bệnh sau khi phẫu thuật có thể bị vàng da và vàng mắt. Các triệu chứng này thường là tạm thời và sẽ cải thiện khi gan phát triển trở lại. Người bệnh cần nằm viện 5 – 10 ngày sau khi cắt gan.
Nút nhánh tĩnh mạch cửa
Trong một số trường hợp, người bệnh sẽ được nút nhánh tĩnh mạch cửa (Portal vein embolisation – PVE) trước phẫu thuật 4 – 8 tuần nếu cần cắt bỏ phần lớn gan mà nhu mô còn lại không thể đảm bảo chức năng.
Tĩnh mạch cửa đưa máu từ dạ dày đến gan rồi chia thành các nhánh trái và phải. Phương pháp PVE sẽ ngăn chặn dòng máu từ tĩnh mạch cửa đến phần gan sắp bị cắt bỏ, khiến dòng máu chuyển hướng đến nuôi dưỡng phần còn lại của gan.
Khi thực hiện PVE, người bệnh sẽ được gây mê toàn thân. Bác sĩ sẽ sử dụng siêu âm hoặc chụp X quang để xác định vị trí đưa ống dẫn qua da vào tĩnh mạch cửa. Bác sĩ sẽ tiêm thuốc cản quang để xác định tĩnh mạch cửa, sau đó nút nhánh tĩnh mạch cửa bên phần gan có u bằng các vật liệu nút mạch như hạt vi cầu, bọt biển gelatin (gelatine spongel) hoặc cuộn kim loại (coil).
Người bệnh sẽ được chụp CT trước và sau thủ thuật để đánh giá kích thước của gan và cân nhắc chỉ định phẫu thuật.
Ghép gan
Ghép gan là phẫu thuật cắt bỏ toàn bộ gan để thay thế bằng một lá gan khỏe mạnh từ người hiến tặng. Phương pháp điều trị này có hiệu quả đối với HCC, nhưng nó thường chỉ được thực hiện ở những trường hợp có 1 khối u đơn lẻ hoặc vài khối u nhỏ. Ghép gan không được chỉ định cho những người bị ung thư biểu mô đường mật.
Yêu cầu của ghép gan là người bệnh cần có thể trạng khỏe mạnh, không hút thuốc, không sử dụng chất kích thích và đã ngừng uống rượu ít nhất 6 tháng.
Gan hiến tặng rất hiếm và việc chờ đợi một lá gan phù hợp có thể mất nhiều tháng. Trong thời gian này, ung thư có thể tiếp tục phát triển. Do đó, hầu hết người bệnh đều sẽ được chỉ định phương pháp đốt nhiệt bằng sóng cao tần hoặc nút mạch hóa chất để kiểm soát ung thư trong thời gian đợi gan phù hợp.
Tuy nhiên, những trường hợp ung thư tiến triển mặc dù đã được điều trị sẽ không có chỉ định ghép gan. Người bệnh sẽ bị loại khỏi danh sách chờ ghép gan và cần điều trị bằng các phương pháp khác.
- Phục hồi sau ghép gan
Sau khi được ghép gan, người bệnh cần nằm viện trong khoảng 3 tuần. Có thể mất từ 3 – 6 tháng để hồi phục sau phẫu thuật.
Người bệnh ghép gan cần sử dụng thuốc ức chế miễn dịch suốt đời để ngăn cơ thể đào thải gan mới. Bác sĩ cũng sẽ chỉ định thuốc kháng sinh để giảm nguy cơ nhiễm trùng.
Phá hủy u gan tại chỗ
Đối với các khối u nhỏ hơn 3 cm, người bệnh có thể được chỉ định các phương pháp phá hủy u gan tại chỗ. Đây là phương pháp tiêu diệt khối u mà không cần phẫu thuật cắt gan, là lựa chọn tốt nhất nếu người bệnh không thể phẫu thuật cắt gan hoặc đang chờ ghép gan. Có nhiều phương pháp phá hủy u gan tại chỗ, phụ thuộc vào kích thước, vị trí và hình dạng của khối u.
- Đốt nhiệt bằng sóng cao tần (Radiofrequency thermal ablation – RF)
Phương pháp này sử dụng nhiệt từ sóng cao tần để tiêu diệt khối u. RF có thể được thực hiện tại phòng chụp X-quang (người bệnh được gây tê cục bộ) hoặc tại phòng mổ (người bệnh được gây mê toàn thân). Bác sĩ sẽ đưa một cây kim nhỏ qua da để đưa sóng cao tần tới khối u dưới hướng dẫn của CT hoặc siêu âm.
Phương pháp RF thực hiện trong 1 – 2 giờ. Sau điều trị, người bệnh cần ở lại bệnh viện qua đêm. Các tác dụng phụ của RF là đau, buồn nôn hoặc sốt, nhưng các triệu chứng này có thể được kiểm soát bằng thuốc.
- Tiêm ethanol qua da
Tiêm ethanol qua da là phương pháp tiêm cồn nguyên chất (ethanol) vào khối u. Phương pháp này được chỉ định trong một số trường hợp không thể điều trị bằng các phương pháp phá hủy u gan tại chỗ khác. Bác sĩ sẽ gây tê cục bộ vị trí chọc kim, sau đó đưa kim vào khối u dưới hướng dẫn của siêu âm. Phương pháp này có thể được thực hiện nhiều lần. Các tác dụng phụ của tiêm ethanol qua da là đau hoặc sốt, nhưng các triệu chứng này có thể được kiểm soát bằng thuốc.
- Phương pháp áp lạnh
Phương pháp áp lạnh tiệu diệt các tế bào ung thư bằng nhiệt độ rất thấp. Đây là phương pháp điều trị không phổ biến, chỉ được sử dụng trong một số trường hợp nhất định. Người bệnh sẽ được gây mê toàn thân, sau đó bác sĩ sẽ rạch một đường nhỏ trên bụng và đưa đầu dò qua đường rạch vào khối u. Đầu dò có nhiệt độ rất thấp, làm đóng băng và tiêu diệt các tế bào ung thư. Phương pháp áp lạnh được thực hiện trong khoảng 60 phút. Sau điều trị, người bệnh thường phục hồi nhanh hơn so với phẫu thuật cắt gan, nhưng nó vẫn có nguy cơ chảy máu và làm tổn thương đường mật.
Nút mạch hóa chất (Transarterial chemoembolisation – TACE)
Hóa trị là phương pháp điều trị ung thư phổ biến, sử dụng thuốc để tiêu diệt hoặc làm tổn thương tế bào ung thư. Tuy nhiên, hóa trị truyền thống hiếm khi được sử dụng cho bệnh ung thư gan nguyên phát. Thay vào đó, phương pháp nút mạch hóa chất (TACE) sẽ đưa trực tiếp thuốc với nồng độ cao vào khối u. Nó thường được sử dụng cho những người không thể phẫu thuật hoặc đang chờ ghép gan. Sau 6 tuần thực hiện TACE, người bệnh sẽ được chụp CT hoặc MRI để đánh giá hiệu quả điều trị.
- Quy trình thực hiện TACE
- Trước khi thực hiện TACE, người bệnh sẽ được gây tê cục bộ hoặc gây mê toàn thân.
- Bác sĩ sẽ rạch một đường nhỏ ở bẹn, sau đó đưa ống thông (catheter) qua đường rạch vào động mạch gan.
- Hóa chất được đưa vào gan qua catheter. Các hạt vi cầu hoặc bọt biển gelatin cũng được đưa vào động mạch gan để chặn dòng máu đến nuôi dưỡng khối u, làm khối u nhỏ lại hoặc ngừng phát triển. Trong một số trường hợp, bác sĩ có thể kết hợp đưa hóa chất và vật liệu nút mạch tới khối u cùng một lúc.
- Sau khi thực hiện TACE, người bệnh phải nghỉ ngơi trong khoảng 4 tiếng và cần nằm viện trong vài ngày.
- Tác dụng phụ của TACE
Thông thường, người bệnh sẽ bị sốt vào ngày đầu tiên sau thực hiện TACE, triệu chứng này thường sẽ nhanh chóng thuyên giảm. Người bệnh cũng có thể cảm thấy hơi đau nhưng triệu chứng này có thể được kiểm soát bằng thuốc giảm đau. Một số người có thể thấy mệt mỏi hoặc xuất hiện các triệu chứng giả cúm trong 1 tuần sau điều trị.
Xạ trị
Xạ trị không phải là phương pháp điều trị ung thư gan nguyên phát phổ biến. Tuy nhiên, 2 phương pháp xạ trị dưới đây có thể được chỉ định trong một số trường hợp cụ thể.
- Xạ trị trong chọn lọc (SIRT)
Xạ trị trong chọn lọc (Selective internal radiation therapy – SIRT) là một phương pháp xạ trị nhằm tiêu diệt chính xác các tế bào ung thư gan. SIRT được chỉ định trong các trường hợp HCC không thể phẫu thuật.
- Xạ trị lập thể định vị thân (SBRT)
Xạ trị lập thể định vị thân (Stereotactic body radiation therapy – SBRT) sử dụng máy điều khiển các tia bức xạ năng lượng cao đi từ bên ngoài cơ thể để chiếu vào khối u ở gan. SBRT có thể được chỉ định cho một số trường hợp HCC có khối u nhỏ không thể phẫu thuật cắt gan.
Liệu pháp nhắm trúng đích
Những trường hợp HCC giai đoạn tiến triển hoặc đang tham gia thử nghiệm lâm sàng có thể được chỉ định liệu pháp nhắm trúng đích (Targeted therapy). Các loại thuốc này tấn công khối u theo các cơ chế đặc biệt để ngăn khối u phát triển.
Sorafenib (Nexavar) là thuốc điều trị nhắm trúng đích đầu tiên được chấp thuận để điều trị HCC giai đoạn tiến triển. Thuốc được dùng bằng đường uống với liều 4 viên/ngày, chia 2 lần.
Các tác dụng phụ của Sorafenib bao gồm: phát ban, tiêu chảy, mệt mỏi và tăng huyết áp. Những tác dụng phụ này có thể được kiểm soát mà không cần phải ngừng uống thuốc. Người bệnh cần được bác sĩ tư vấn về các biện pháp kiểm soát tác dụng phụ trong suốt quá trình điều trị.
Nói chung, việc điều trị bằng liệu pháp nhắm trúng đích sẽ được duy trì nếu tình trạng bệnh cải thiện. Nếu ung thư gan tiếp tục tiến triển dù đã điều trị bằng sorafenib, bác sĩ có thể chỉ định thêm thuốc nhắm trúng đích khác. Ngoài ra, người bệnh có thể tham gia thử nghiệm lâm sàng để được điều trị bằng các loại thuốc mới.
Thuốc điều trị HCC giai đoạn tiến triển ngày càng có nhiều thay đổi và các phương pháp điều trị mới có thể được thực hiện trong tương lai gần, đặc biệt là các loại thuốc điều trị miễn dịch để kích thích hệ thống miễn dịch của cơ thể chống lại ung thư.
Ung thư biểu mô đường mật
Ung thư biểu mô đường mật là một dạng ung thư gan nguyên phát ít phổ biến hơn HCC, chiếm 10 – 15% các trường hợp ung thư gan nguyên phát trên thế giới. Loại ung thư này bắt nguồn từ tế bào biểu mô lót các ống dẫn mật từ gan đến túi mật và ruột. Các triệu chứng của ung thư biểu mô đường mật tương tự như HCC.
Yếu tố nguy cơ – Yếu tố nguy cơ chính của ung thư biểu mô đường mật là tình trạng viêm đường mật mạn tính. Ngoài ra, một số bệnh lý ở gan như viêm gan và gan nhiễm mỡ là yếu tổ nguy cơ của ung thư biểu mô đường mật (tương tự HCC). Bên cạnh đó, viêm xơ đường mật nguyên phát hoặc viêm loét đại tràng cũng làm tăng nguy cơ ung thư biểu mô đường mật.
Chẩn đoán – Các xét nghiệm chính giúp chẩn đoán ung thư biểu mô đường mật là siêu âm và MRI. Trong một số trường hợp, người bệnh có thể được chụp MRI mật tụy (magnetic resonance cholangiopancreatography – MRCP) để đánh giá chi tiết hệ thống đường mật. Một thăm dò khác là nội soi mật tụy ngược dòng (Endoscopic retrograde cholangiopancreatography – ERCP). Phương pháp này sử dụng ống nội soi có gắn camera để quan sát đường mật và cũng có thể kết hợp với đặt stent đường mật. Ngoài ra, xét nghiệm chất chỉ điểm ung thư CA 19-9 tăng cũng có thể định hướng tới ung thư biểu mô đường mật.
Giai đoạn – Ung thư biểu mô đường mật được phân loại bằng hệ thống TNM dựa trên kích thước của khối u (Tumor – T), số lượng hạch bạch huyết di căn (Nodes – N) và tình trạng di căn đến các cơ quan khác (Metastasis – M).
Điều trị – Các phương pháp điều trị ung thư biểu mô đường mật có thể là phẫu thuật cắt gan bán phần hoặc đặt stent đường mật. Hóa trị cũng là một phương pháp điều trị phổ biến. Phương pháp này sử dụng các thuốc đường tĩnh mạch để tiêu diệt hoặc làm tổn thương các tế bào ung thư, ngăn chặn ung thư phát triển hoặc di căn. Xạ trị ngoài có thể được chỉ định cho ung thư biểu mô đường mật giai đoạn tiến triển. Phương pháp này sử dụng tia bức xạ để tiêu diệt hoặc làm tổn thương các tế bào ung thư. Bên cạnh đó, xạ trị trong cũng là một phương pháp điều trị ung thư biểu mô đường mật.
Điều trị chăm sóc giảm nhẹ
 Người bệnh mắc ung thư gan cần được chăm sóc cả về thể chất lẫn tinh thần. Nguồn ảnh: Verywellhealth.com
Người bệnh mắc ung thư gan cần được chăm sóc cả về thể chất lẫn tinh thần. Nguồn ảnh: Verywellhealth.comNếu ung thư gan nguyên phát ở giai đoạn tiến triển hoặc tái phát sau khi điều trị, bác sĩ sẽ tư vấn cho người bệnh về các phương pháp điều trị chăm sóc giảm nhẹ để cải thiện các triệu chứng của ung thư.
Điều trị chăm sóc giảm nhẹ nhằm mục đích kiểm soát các triệu chứng chứ không cố gắng chữa khỏi bệnh. Biện pháp này có thể được chỉ định cho người bệnh ung thư giai đoạn cuối để cải thiện chất lượng cuộc sống.
Điều trị chăm sóc giảm nhẹ có thể làm chậm sự lan rộng của ung thư, hỗ trợ giảm đau và cải thiện các triệu chứng khác. Các phương pháp điều trị chăm sóc giảm nhẹ có thể là hóa trị, liệu pháp nhắm trúng đích, một số loại thuốc khác hoặc đặt stent đường mật.
Chăm sóc giảm nhẹ còn nhằm đáp ứng các nhu cầu về thể chất, tinh thần và chia sẻ của người bệnh.
Kết luận
Ung thư gan nguyên phát là ung thư bắt nguồn từ các tế bào ở gan. Loại ung thư gan phổ biến nhất là ung thư biểu mô tế bào gan (HCC). Loại ung thư gan ít gặp hơn là ung thư biểu mô đường mật.
Các xét nghiệm chính để chẩn đoán ung thư gan là xét nghiệm máu và các xét nghiệm chẩn đoán hình ảnh như siêu âm, chụp CT hoặc MRI. Sinh thiết gan không phải là tiêu chuẩn bắt buộc nhưng có thể được chỉ định trong một số trường hợp.
Để xác định giai đoạn ung thư gan, bác sĩ sẽ dựa vào kết quả của các xét nghiệm cũng như chức năng gan (theo thang điểm Child-Pugh). HCC thường được phân loại bằng hệ thống phân loại bệnh ung thư gan Barcelona (BCLC).
Các phương pháp điều trị ung thư gan phổ biến nhất bao gồm:
- Đốt nhiệt bằng sóng cao tần (RF)
- Nút mạch hóa chất (TACE)
Một số phương pháp điều trị khác là:
- Phẫu thuật cắt gan hoặc ghép gan
- Tiêm ethanol qua da hoặc áp lạnh đối với các khối u nhỏ
- Xạ trị trong chọn lọc (SIRT) hoặc xạ trị lập thể định vị thân (SBRT)
- Liệu pháp nhắm trúng đích như Sorafenib
Xem thêm:



























